Chez les bactéries, les principaux gènes de la voie de biosynthèse de la biotine sont organisés en un opéron. Ce type d’organisation structurale des gènes en opérons n’existe pas chez les plantes où les gènes de la voie de biosynthèse de la biotine sont dispersés dans le génome. Seuls, les gènes BIO3 et BIO1 sont adjacents chez toutes les plantes dont le génome a été séquencé à ce jour et codent deux étapes successives de la voie de synthèse (Figure 1). Chez la plante modèle Arabidopsis thaliana ces gènes codent une protéine fusion BIO3-BIO1 et certaines observations suggèrent que l’origine de ce gène bifonctionnel provient de la fusion de deux gènes procaryotiques, fusion qui serait survenue très tôt dans l’évolution des premiers eucaryotes.
Figure 1 : Réactions catalysées par BIO3-BIO1. Le domaine BIO1 catalyse la réaction DAPA aminotranférase dépendante du PLP, à partir de KAPA et d’AdoMet comme donneur d’amine. Le domaine BIO3 catalyse la réaction DTB synthétase qui est une carboxylation ATP-dépendante. La desthiobiotine étant le précurseur direct de la biotine. AdoMet, S-adénosylméthionine ; PLP, pyridoxal 5’-phosphate ; KAPA, acide kéto amino pélargonique ; DAPA, acide diamino pélargonique ; DTB, desthiobiotine.
Nous avons, en collaboration avec le Laboratoire de Cristallogenèse et Cristallographie des Protéines de l’IBS, biochimiquement caractérisé la protéine BIO3-BIO1 d’
Arabidopsis puis résolu sa structure tridimensionnelle en l’absence et en présence de ses différents ligands (substrats, produits et cofacteurs) (
Figure 2). Cette étude montre qu’au cours de la réaction, le DAPA (l’intermédiaire réactionnel des réactions catalysées par l’enzyme) est transféré directement et rapidement du site catalytique du domaine BIO1 où il est synthétisé, vers celui du domaine BIO3 où il est ensuite métabolisé en desthiobiotine (le précurseur direct de la biotine), sans diffuser dans le milieu environnant. En l’absence des autres substrats du domaine BIO3, le DAPA produit est séquestré au niveau du site BIO1, ce qui permet une bonne coordination des deux réactions.
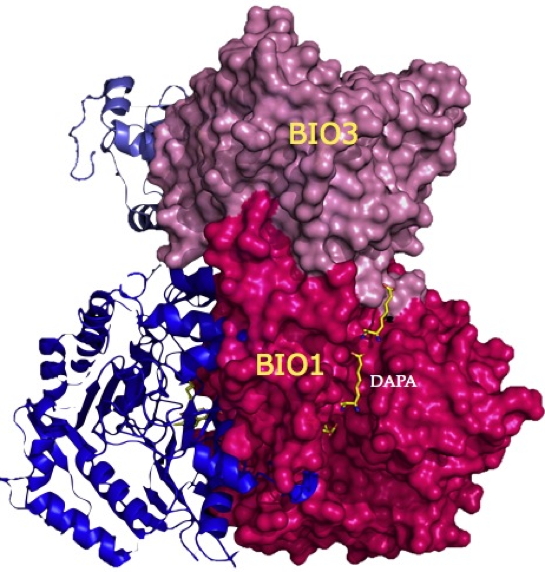
Figure 2 : Structure tridimensionnelle de l’enzyme bifonctionnelle BIO3-BIO1 d’Arabidopsis thaliana. Sont visibles les deux domaines BIO1 et BIO3, ainsi que des molécules de DAPA, l’intermédiaire réactionnel, migrant du site BIO1 ou il est synthétisé vers le site BIO3 ou il sera transformé en DTB, le précurseur direct de la biotine.
La résolution de la structure de l’enzyme met en évidence la présence à sa surface d’un sillon reliant les deux sites catalytiques. Cette structure, absente en surface des enzymes bactériennes correspondantes (enzymes mono-fonctionnelles), pourrait constituer la voie de passage du DAPA. Pour tester cette hypothèse les chercheurs de l’équipe ont substitué certains acides aminés situés au fond de ce sillon par d’autres, plus volumineux, afin d’entraver le cheminement du DAPA. Ces mutations ont eu pour conséquence d’empêcher la communication des deux domaines fonctionnels et ont conduit à un relargage et donc à une diffusion du DAPA produit, réduisant ainsi de manière dramatique le couplage des deux réactions catalysées par BIO3-BIO1 et par conséquent l’efficacité catalytique du système. Les deux domaines ayant des vitesses catalytiques très différentes et la réaction catalysée par le domaine BIO1 étant totalement réversible, un tel mécanisme de «
channelling » pourrait constituer un moyen efficace d'empêcher cette réaction de fonctionner dans le mauvais sens.
Il existe peu d’exemples documentés d’enzymes bifonctionnelles catalysant deux étapes successives ou non d’une même voie de biosynthèse. Ainsi, une vingtaine d'enzymes seulement sont décrites chez les plantes, ces enzymes étant impliquées essentiellement dans le métabolisme des vitamines, des acides aminés et des lipides. Rares sont celles cependant, tous règnes confondus, à avoir été caractérisées de manière exhaustive et très peu d’informations sont disponibles sur les mécanismes réactionnels de ces enzymes, notamment ceux permettant d’assurer le transit des intermédiaires réactionnels d’un site catalytique à l’autre. De telles informations sont pourtant essentielles à une meilleure compréhension de la régulation des voies métaboliques impliquées, notamment dans l’optique d’optimiser l’efficacité catalytique des enzymes qui la constituent afin d’améliorer les procédés de production de molécules à haute valeur ajoutée, ou de permettre le «
design » d’inhibiteurs spécifiques à des fins thérapeutiques ou phytosanitaires.
Un opéron est un groupement de gènes qui sont transcrits ensemble en ARN messager.