Les cellules se déplacent et se déforment en utilisant la force développée par leur cytosquelette d’actine. Ce cytosquelette est fait d’un grand nombre de filaments, formant un réseau dont la composition et la dynamique sont très complexes et en perpétuel réarrangement.
Pour comprendre cette dynamique, nous avons, en collaboration avec Cécile Sykes de l’Institut Curie (Paris) utilisé un système biomimétique permettant de reconstituer
in vitro un tel réseau d'actine. Ce système est composé de monomères d’actine, d’un complexe qui initie et réticule des filaments d'actine (Arp2/3), d’un activateur de ce complexe qui recouvre la surface de billes de polystyrène, et d’une protéine qui interrompt l’élongation de ces polymères d’actine (la protéine de coiffe CP). Dans ce système biomimétique, le réseau d’actine qui se développe à la surface des billes est capable de les propulser.
Cette nouvelle étude vise à caractériser la production de forces générées par les réseaux de filaments d’actine afin de mieux en comprendre la complexité en combinant la reconstitution du mouvement de ces billes et des modèles biophysiques. Tout d’abord, nous avons modélisé la cinétique de croissance de réseaux de filaments à partir de filaments d’actine isolés positionnés à la surface d’une bille (
Figure A). Chaque filament isolé est à l’origine d’un réseau réticulé qui se développe grâce i) à l’élongation des filaments par polymérisation des monomères d’actine et ii) par leur branchement donnant lieu à une structure arborescente. Ceci est rendu possible par le complexe Arp2/3 qui initie et réticule des filaments d'actine et par l’activateur de ce complexe fixé à la surface des billes (
Figure B). Néanmoins l'élongation de ces filaments est limitée par l’action de la protéine de coiffe conduisant à la densification des réseaux. Pour une combinaison favorable des concentrations de Arp2/3 et de CP, il a formation d’un gel d’actine. Ces étapes (initiation, réticulation et élongation) sont simples à simuler par un modèle peu coûteux en temps de calcul et ceci pour un nombre réaliste d’environ 10 000 filaments par bille.
Lorsque la bille est entièrement recouverte par l’enchevêtrement des différents réseaux réticulés, il devient nécessaire d’intégrer au modèle
cinétique, un autre
modèle rendant compte de la mécanique des filaments. Nous adoptons une description ‘
coarse grained’ dans laquelle les réseaux arborescents sont représentés par des
points, et les interactions à l’interface entre deux réseaux par des
ressorts (
Figure C). On peut ainsi "oublier" les détails (filaments) pour se concentrer sur la dynamique globale des réseaux. Les forces dues à l’allongement des filaments (calculées par le modèle cinétique) sont appliquées aux ressorts (modèle ‘
coarse grained’) et les mettent sous tension (
Figures C et D). Lorsque l’extension d’un des ressorts dépasse un certain seuil, une fissure apparaît. En se propageant, cette fissure conduit à une brisure de symétrie (ou ouverture) du réseau global entourant la bille et
in fine, à la propulsion de la particule (
Figure D).
Cette synergie expérience-modèle a permis d’identifier et de formuler les principes gouvernant la dynamique et l’organisation du cytosquelette. Ces recherches permettent de mieux comprendre le rôle de cette dynamique dans les cellules (conditions normales et pathologiques). Par exemple ces études mettent en évidence les conséquences des dysfonctionnements mécaniques intracellulaires pour des pathologies aussi graves que le cancer.
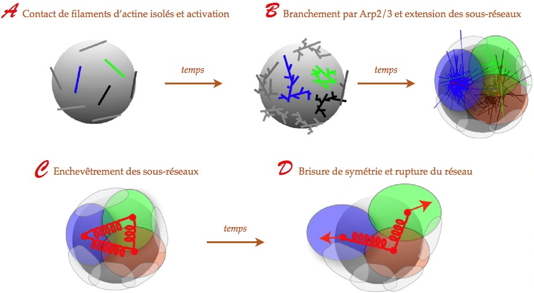
Figure. Différentes étapes de la croissance du réseau d’actine à la surface d’une bille fonctionnalisée.
A. Génération de sous-réseaux en différents points sur la bille.
B. Extension, branchement et enchevêtrement des sous-réseaux.
C. Lorsque l’enchevêtrement est complet, les interactions entre sous-réseaux sont modélisées par des ressorts.
D. La force due à la polymérisation de monomères dans le réseau parvient à rompre l’un des ressorts.